O produto é fabricado pela indústria farmacêutica Wyeth
 |
| © Shutterstock |
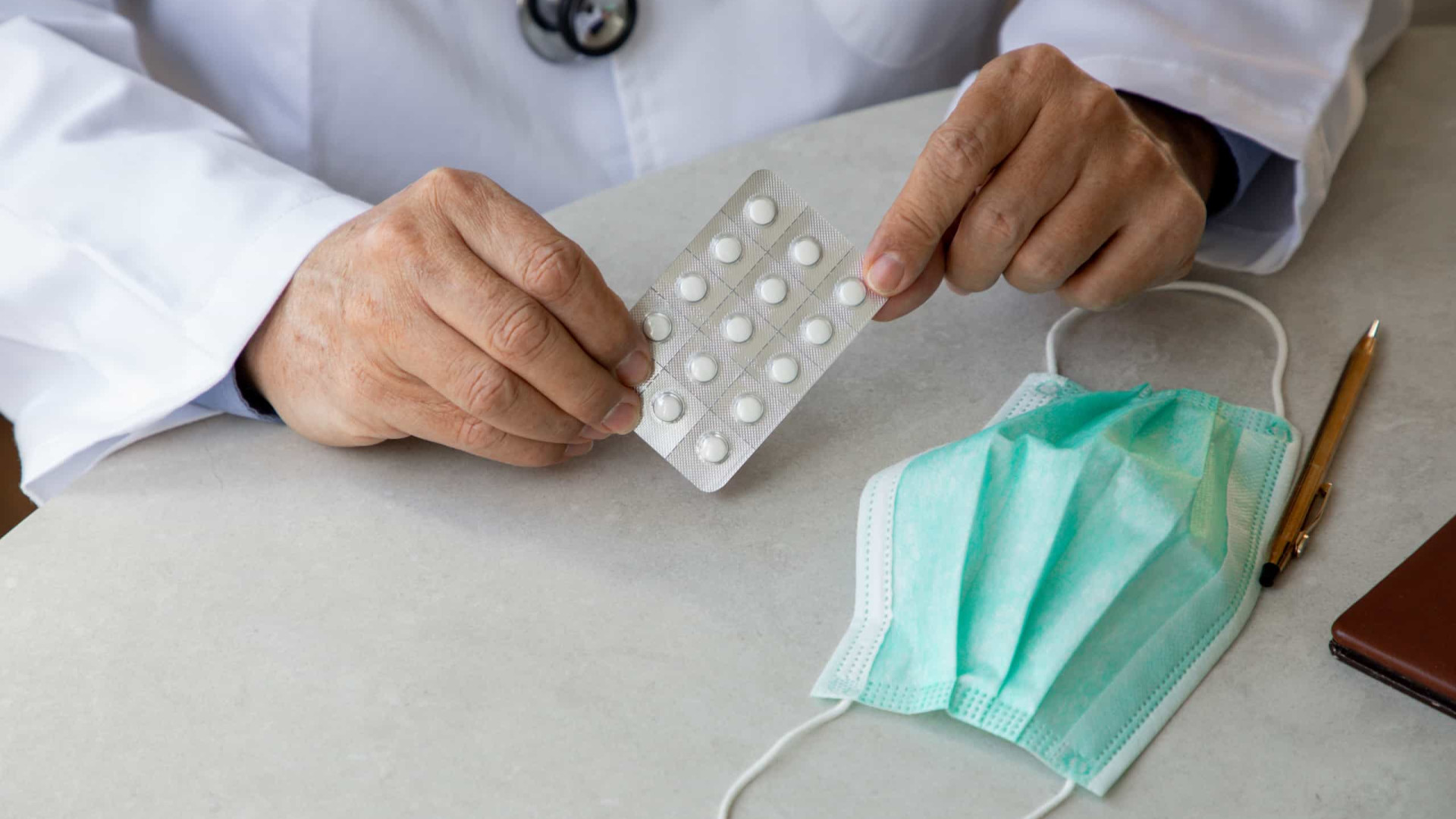
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou nesta quarta-feira (30) a autorização, em caráter emergencial, do medicamento para a covid-19 Paxlovid, que compreende o uso combinado dos remédios nirmatrelvir e ritonavir. O produto é fabricado pela indústria farmacêutica Wyeth.
O medicamento é indicado para adultos que testaram positivo, que não precisam de oxigênio e que têm risco de evolução para quadros graves da doença. Seu principal efeito é no combate à piora nas condições de saúde das pessoas infectadas.
O remédio é de uso individual oral, mas não é indicado para pessoas abaixo de 18 anos de idade. Também não há indicação para gestantes ou pessoas que podem ou pretendem engravidar durante o tratamento.
A diretora da Anvisa Meiruze Souza Freitas avaliou que os benefícios da liberação do medicamento superam os riscos. Ela acrescentou que a antecipação de produtos para tratar a covid-19 está alinhada à garantia de possibilidades de tratamento contra a doença, considerando a situação da pandemia no Brasil.
“Com a pandemia enfrentamos desafios sem precedentes. Melhorar essa lacuna é prioridade de saúde pública. A disponibilidade de medicamentos essenciais continua insuficiente por motivos diversos, como preços altos, compra e distribuição deficientes, qualidade incerta do produto e prescrição inadequada”, disse Meiruze Freitas.
Já o diretor da Anvisa Rômison Mota destacou que não se trata de um medicamento para prevenção, e que já houve aprovação em outros países como Estados Unidos, Canadá e México.
O diretor da Anvisa Alex Campos lembrou que não é um substituto da vacina, que está disponível gratuitamente, enquanto o Paxlovid, a princípio, será comercializado, dependendo de poder aquisitivo para o consumo.
A diretora Cristiane Jourdan assinalou que os dados evidenciam benefícios superando os riscos e que as medidas para gerenciamento de risco estão compatíveis com as medidas utilizadas no mercado.
A equipe técnica da Anvisa apontou riscos a serem monitorados no uso concomitante com outros produtos. “Foram feitas exigências de incluir na bula as contraindicações de uso concomitante com o medicamento apalutamida”, informou a gerente de Farmacovigilância, Helaine Capucho.
A gerente listou pontos colocados pela Anvisa, incorporados no plano de gestão de riscos e na bula do remédio. A equipe da Anvisa determinou que seja feita carta a profissionais de saúde para orientação sobre usos do Paxlovid com outros remédios e dos cuidados necessários. Também foi requisitado que a empresa disponibilize informações acerca do uso do produto no Brasil para monitorar sua aplicação e eventuais eventos adversos.
“Incluímos o compromisso de apresentar relatórios de estudos clínicos e não-clínicos e informar trimestralmente a situação regulatória em outros países”, disse o gerente geral de Medicamentos e Produtos Biológicos da Anvisa, Gustavo Mendes.
VIA...NOTÍCIAS AO MINUTO

Nenhum comentário:
Postar um comentário
Os comentários são pessoais, é não representam a opinião deste blog.
Muito obrigado, Infonavweb!